QC制药企业实验室管理整体要求与企业管理咨询实践
在药品生产领域,质量控制(QC)实验室是确保药品安全、有效、质量均一的核心环节。其管理水平直接关系到企业的合规运营、产品质量信誉与市场竞争力。一套系统、科学、合规的实验室管理整体要求,不仅是监管机构的强制规定,更是企业自身发展的内在需求。企业管理咨询在此过程中扮演着至关重要的角色,协助企业构建并持续优化这一管理体系。
一、QC制药企业实验室管理的核心整体要求
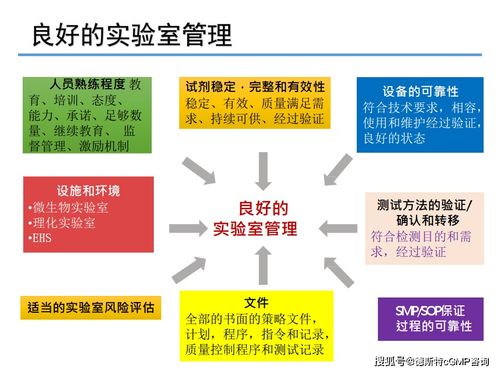
QC实验室管理是一个系统工程,其整体要求可概括为以下几个相互关联的维度:
1. 法规符合性基础:
这是所有要求的基石。实验室必须严格遵循《药品生产质量管理规范》(GMP)、中国药典、ICH Q7等相关法律法规及行业指南。这涵盖了从人员资质、设施环境、设备管理到检验方法、数据完整性的方方面面。任何操作都必须在既定的、经过验证的规程框架内进行。
2. 组织与人员管理:
实验室应建立清晰的组织架构,明确各岗位职责与权限。关键人员(如实验室负责人)必须具备相应的教育背景、专业培训和丰富的实践经验。所有人员均需接受持续的GMP、安全及岗位操作培训,并建立完善的培训档案与考核机制。
3. 设施、环境与设备管理:
* 设施与环境: 实验室布局应合理,防止交叉污染和混淆。对温湿度、洁净度、生物安全等有特殊要求的区域(如无菌检查室、微生物限度室)必须进行严格控制和持续监测。
- 设备管理: 所有用于检验的仪器、仪表、量具均需建立台账,实施唯一的身份标识。必须制定详细的采购、验收、使用、清洁、维护、校准和报废标准操作规程(SOP)。关键仪器(如HPLC、GC)需进行安装确认(IQ)、运行确认(OQ)和性能确认(PQ)。
4. 文件与记录体系:
建立涵盖所有操作和管理活动的文件系统,包括质量标准、检验规程、SOP、记录与报告等。所有记录(包括纸质和电子数据)必须遵循 “ALCOA+”原则(可追溯、清晰、同步、原始、准确、完整、一致、持久、可用),确保数据完整性。文件的起草、审核、批准、分发、修订和废止必须受控。
5. 物料与试剂管理:
对标准品、对照品、试剂、实验用水、培养基等建立严格的管理程序,包括采购、接收、标识、储存(如规定储存条件)、使用和有效期管理。标准品和关键试剂需进行适用性检查。
6. 检验过程控制:
所有检验方法必须经过验证或确认。样品管理需确保其代表性、完整性和可追溯性。检验操作必须严格按照批准的规程进行。对出现的偏差(OOS/OOT/OOE)必须启动正式的调查程序,查明根本原因并采取纠正预防措施(CAPA)。
7. 质量控制与保证的衔接:
QC实验室是质量保证(QA)体系的重要支撑。实验室需定期进行趋势分析(如环境监测、检验结果趋势),为产品质量回顾和工艺改进提供数据支持。积极参与变更控制、供应商管理、验证活动等质量保证环节。
8. 安全与文化:
建立实验室安全管理制度,涵盖化学品安全、生物安全、消防安全、废弃物处理等。培育以质量为核心、实事求是、持续改进的实验室文化,鼓励员工主动报告偏差和潜在风险。
二、企业管理咨询在优化实验室管理中的价值与实践
面对复杂且动态的法规环境与管理要求,许多制药企业,特别是中小型企业或处于快速发展期的企业,需要借助外部专业的企业管理咨询力量来系统提升实验室管理水平。咨询实践通常包括:
1. 现状诊断与差距分析:
咨询顾问通过现场观察、文件审核、人员访谈等方式,全面评估实验室现有管理体系与GMP等法规要求及行业最佳实践之间的差距,出具详细的诊断报告,明确改进的优先级。
2. 管理体系设计与流程再造:
基于诊断结果,协助企业设计或优化实验室的组织架构、职责分工。梳理并重构核心业务流程(如样品流转、偏差调查、设备管理、数据管理),编写或修订全套、层级清晰的SOP文件体系。
3. 数据完整性专项提升:
针对当前监管重点,顾问会专项审查实验室的纸质和电子数据流,识别在数据生成、记录、处理、审核、报告、存储等各环节的漏洞,帮助实施合规的计算机化系统验证,建立有效的数据生命周期管理策略。
4. 人员能力建设与培训:
设计并实施针对性的培训课程(如GMP高级课程、分析方法验证、偏差调查技巧、数据完整性意识),提升团队的专业素养和合规意识。有时还包括协助建立更有效的绩效考核与激励机制。
5. 迎检准备与模拟审计:
在官方检查或客户审计前,咨询顾问可以扮演审计官角色,进行全流程的模拟审计,帮助企业提前发现并整改问题,训练团队应对审计的能力,从而提升正式迎检的信心和通过率。
6. 持续改进机制构建:
辅导企业建立基于风险的、主动的持续改进文化。协助搭建有效的质量指标监控体系、管理评审机制和CAPA系统,确保实验室管理体系能够自我完善,动态适应内外部变化。
###
QC制药企业实验室管理的整体要求是一个严谨、细致、环环相扣的合规与质量网络。达到并超越这些要求,不能仅靠被动应对检查,而需要企业高层的高度重视、资源的持续投入以及管理体系的系统构建。专业的企业管理咨询机构凭借其深厚的行业知识、丰富的实践经验和客观的第三方视角,能够高效地帮助企业弥补短板、构建稳健的实验室质量管理体系,从而为生产出安全有效的药品奠定最坚实的基石,最终护航企业在激烈的市场竞争中行稳致远。
如若转载,请注明出处:http://www.ftpxq.com/product/16.html
更新时间:2026-06-03 22:21:32